Fosforescenţă este luminiscența care apare atunci când energie este furnizat de radiatie electromagnetica, de obicei lumină ultravioletă. Sursa de energie lovește un electron al unui an atom dintr-o stare energetică inferioară într-o stare energetică „excitată”; atunci electronul eliberează energia sub formă de lumina vizibila (luminiscență) atunci când se întoarce la o stare de energie mai mică.
Cheltuieli cheie: Fosforescență
- Fosforescența este un tip de fotoluminescență.
- În fosforescență, lumina este absorbită de un material, ridicând nivelul de energie al electronilor într-o stare excitată. Cu toate acestea, energia luminii nu se potrivește cu energia stărilor excitate permise, astfel încât fotografiile absorbite rămân blocate într-o stare triplă. Tranzițiile către o stare de energie mai mică și mai stabilă necesită timp, dar atunci când apar, lumina este eliberată. Deoarece această eliberare are loc lent, un material fosforescent pare să strălucească în întuneric.
- Exemple de materiale fosforescente includ stele strălucitoare în întuneric, unele semne de siguranță și vopsea strălucitoare. Spre deosebire de produsele fosforescente, pigmenții fluorescenți încetează să strălucească odată ce sursa de lumină este îndepărtată.
- Deși numit pentru strălucirea verde a elementului fosfor, fosforul strălucește de fapt din cauza oxidării. Nu este fosforescent!
Explicație simplă
Fosforescența eliberează energia stocată încet în timp. Practic, materialul fosforescent este „încărcat” expunându-l la lumină. Apoi, energia este păstrată o perioadă de timp și eliberată lent. Atunci când energia este eliberată imediat după absorbția energiei incidente, procesul se numește fluorescenţă.
Explicația mecanicii cuantice
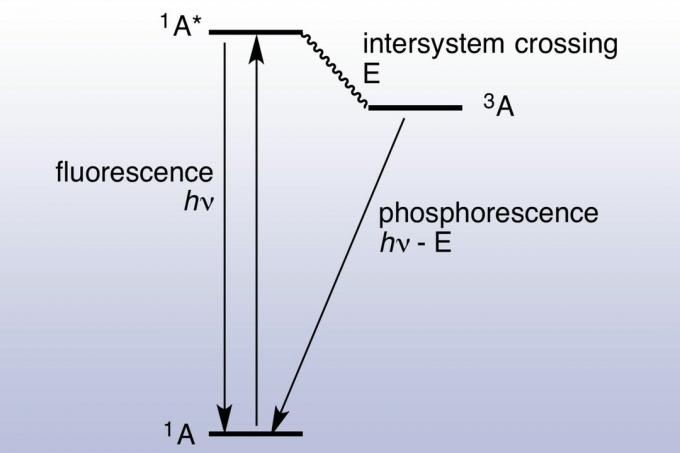
În fluorescență, o suprafață absoarbe și emite un foton aproape instantaneu (aproximativ 10 nanosecunde). Fotoluminiscența este rapidă, deoarece energia fotonilor absorbiți se potrivește cu stările energetice și tranzițiile permise ale materialului. Fosforescența durează mult mai mult (milisecunde până la zile), deoarece electronul absorbit se încrucișează într-o stare excitată, cu o multiplicitate mai mare a spinului. Electronii excitați sunt prinși într-o stare triplă și nu pot folosi decât tranzițiile „interzise” pentru a scădea la o stare de singlet de energie mai mică. Mecanica cuantică permite tranziția interzisă, dar nu sunt cinetice favorabile, astfel încât durează mai mult. Dacă este absorbită suficientă lumină, lumina stocată și eliberată devine suficient de semnificativă pentru ca materialul să pară „strălucitor în întuneric. ”Din acest motiv, materialele fosforescente, ca și materialele fluorescente, apar foarte luminoase sub o lumină neagră (ultravioletă). O diagrama Jablonski este folosită în mod obișnuit pentru a afișa diferența dintre fluorescență și fosforescență.
Istorie
Studiul materialelor fosforescente datează cel puțin din 1602 când italianul Vincenzo Casciarolo a descris un „lapis solaris” (piatră solară) sau „lapis lunaris” (piatră lunară). Descoperirea a fost descrisă în cartea din 1612 a profesorului de filozofie Giulio Cesare la Galla De Phenomenis în Orbe Lunae. La Galla relatează că piatra lui Casciarolo a emis lumină pe ea după ce a fost calcificată prin încălzire. A primit lumină de la Soare și apoi (ca Luna) a dat lumină în întuneric. Piatra era barit impur, deși alte minerale prezintă și fosforescență. Acestea includ unele caro (cunoscut regelui indian Bhoja încă din 1010-1055, redescoperit de Albertus Magnus și din nou redescoperit de Robert Boyle) și topaz alb. Chinezii, în special, au apreciat un tip de fluorit, numit clorofan, care ar afișa luminescența de la căldura corporală, expunerea la lumină sau la frecare. Interesul pentru natura fosforescenței și alte tipuri de luminiscență a dus în cele din urmă la descoperirea radioactivității în 1896.
materiale
Pe lângă câteva minerale naturale, fosforescența este produsă de compuși chimici. Probabil cea mai cunoscută dintre acestea este sulfura de zinc, care a fost folosită în produse încă din anii ’30. Sulfura de zinc emite de obicei o fosforescență verde, deși pot fi adăugați fosfori pentru a schimba culoarea luminii. Fosforii absorb lumina emisă de fosforescență și apoi o eliberează ca o altă culoare.
Mai recent, aluminatul de stronțiu este utilizat pentru fosforescență. Acest compus strălucește de zece ori mai strălucitor decât sulfura de zinc și, de asemenea, își păstrează energia mult mai mult.
Exemple de fosforescență
Printre exemplele obișnuite de fosforescență se numără stele pe care oamenii se află pe pereții dormitorului care strălucesc ore întregi după ce se aprind luminile și se folosesc vopseaua pentru a realiza picturi murale stelare strălucitoare. Deși elementul fosfor strălucește verde, lumina este eliberată de oxidare (chemiluminiscență) și este nu un exemplu de fosforescență.
surse
- Franz, Karl A.; Kehr, Wolfgang G.; Siggel, Alfred; Wieczoreck, Jürgen; Adam, Waldemar (2002). "Materiale luminiscente" în Enciclopedia de chimie industrială a lui Ullmann. Wiley-VCH. Weinheim. doi: 10.1002 / 14356007.a15_519
- Roda, Aldo (2010). Chemiluminiscența și bioluminiscența: trecut, prezent și viitor. Societatea Regală de Chimie.
- Zitoun, D.; Bernaud, L.; Manteghetti, A. (2009). Sinteza cu microunde a unui fosfor cu durată lungă. J. Chem. Educ. 86. 72-75. doi: 10.1021 / ed086p72